|
|
|
|
Neuigkeiten Das Projekt Technik RoboSpatium Unterstützung Stichwortverzeichnis Download Reaktionen Spiele Gadgets Kontakt <<< Korrosionsschutz Batterietypen >>> BatterienElektrochemische ZelleEine elektrochemische Zelle ist eine Anordnung, mit deren Hilfe man elektrische Energie aus chemischen Reaktionen gewinnen kann oder die den Ablauf chemischer Reaktionen durch das Eintragen elektrischer Energie ermöglicht. Wir haben eine elektrochemische Zelle bereits als galvanische Zelle kennen gelernt, die elektrische Energie aus chemischen Reaktionen bereitstellt. Damit ist die galvanische Zelle eine Sonderform der elektrochemischen Zelle. Chemische Reaktionen, die durch die Zufuhr elektrischer Energie ablaufen, werden in den Kapiteln zu Akkumulatoren behandelt. Wie die galvanische Zelle auch, besteht eine elektrochemische Zelle aus mindestens zwei Halbzellen.GleichgewichtsreaktionenDie Reaktionen in einer Halbzelle einer galvanischen Zelle sind Gleichgewichtsreaktionen zwischen verschiedenen Oxidationsstufen der entsprechenden Ionen beziehungsweise Atome. In einer Halbzelle, bestehend aus einer Zinkelektrode in einer Zinksulfatlösung, ist die Halbreaktion gegeben durch:Im Gleichgewichtszustand ändern sich die Konzentrationen der an der Reaktion beteiligten Substanzen im Verlauf der Zeit nicht. Das bedeutet nicht, dass die Reaktion abbricht, sobald der Gleichgewichtszustand erreicht ist,sondern dass die Reaktionsrate der Hinreaktion (Zinkatome gehen als Zink-Kationen in Lösung), gleich der Reaktionsrate der Rückreaktion ist (Zink-Kationen werden an der Elektrodenoberfläche als Zinkatome abgeschieden). Andersherum: wenn sich die Konzentration des Edukts oder eines der Produkte ändert, ändert sich damit die Reaktionsrate der Hin- oder Rückreaktion ebenfalls. Wenn wir zum Beispiel die im Verlauf der Hinreaktion gebildeten Elektronen "absaugen" würden, stiege die Reaktionsrate der Hinreaktion, was zu der Bildung weiterer Elektronen führt: Würden wir hingegen umgekehrt zusätzliche Elektronen "injizieren", so stiege damit die Rate der Rückreaktion, womit Elektronen verbraucht und elementares Zink gebildet wird: Es ist schwierig, Elektronen in einer Halbzelle einfach "abzusaugen" oder zu"injizieren", weil wir damit die gesamte Halbzelle im Verlauf dieses Vorganges positiv beziehungsweise negativ aufladen müssen. Um das einfacher machen zu können, benötigen wir eine weitere Halbzelle, wie im Kapitel zur galvanischen Zelle beschrieben. Ist das Normalpotential der zweiten Halbzelle höher, werden Elektronen aus der Zink-Halbzelle "abgesaugt" und Anionen zugeführt, um die Ladungsbilanz auszugleichen. Aus diesem Grund steigt die Rate der Hinreaktion, sobald beide Halbzellen durch eine Salzbrücke und einen Draht miteinander verbunden werden. Ist das Normalpotential der zweiten Halbzelle geringer, werden Elektronen in die Zinkelektrode "injiziert" und Sulfat-Anionen aus dem Zinksulfat-Elektrolyten abgeführt, um die Ladung auszugleichen. Nun steigt die Rate der Rückreaktion. KapazitätEine galvanische Zelle verwandelt chemische in elektrische Energie. Um die Energiemenge berechnen zu können, die in einer einzelnen galvanischen Zelle gespeichert ist, müssen wir die Zahl der Atome beziehungsweise Ionen in jeder Halbzelle kennen. Anstatt die Atome zu zählen, ist es viel einfacher, die Masse aller Atome in einer Elektrode beziehungsweise der Ionen in dem Elektrolyten zu bestimmen. Die Gesamtmasse der Elektrode dividiert durch die Masse eines einzelnen Atoms ergibt die Anzahl der Atome, aus der die Elektrode besteht. Die Massen einzelner Atome sind in der Tabelle des Periodensystems aufgelistet, angegeben in atomaren Masseneinheiten (u). 1u ist als ein zwölftel der Ruhemasse eines ungebundenen Kohlenstoff-Isotops 12C im Grundzustand festgelegt und entspricht einem Wert von 1,660538782(83)*10-27 kg.Eine in der Chemie oft genutzte Maßeinheit ist das Mol, das als die Stoffmenge definiert ist, die aus ebenso vielen Einzelteilchen (z.B. Atome, Moleküle, Ionen, Elektronen) besteht, wie Atome in 12g des Kohlenstoffisotops 12C enthalten sind. Umgekehrt ist die Anzahl der Atome in 12g des Kohlenstoffisotops 12C gegeben durch die Avogadro Konstante (NA), deren experimentell bestimmter Wert 6,02214179(30)*1023 mol-1 ist. Berechnen wir die chemische Energie, die in einer galvanischen Zink-Kupfer-Zelle steckt. Im Verlauf der Energieumwandlung löst sich die Zinkelektrode in Zink-Kationen auf und Cu2+-Ionen werden als elementares Kupfer abgeschieden. Nehmen wir an, zu Beginn des Entladevorgangs betrage die Masse der Zinkelektrode 50g. Die Masse eines einzelnen Zinkatoms beträgt 65,409u, womit die Anzahl der Zinkatome In der anderen Halbzelle werden Cu2+-Ionen zu Kupferatomen reduziert. Damit ergibt sich ein Verhältnis von 1:1 zwischen Zinkatomen und Cu2+-Ionen, d.h. wir benötigen die gleiche Anzahl an Kupferionen um die Zinkelektrode komplett aufzulösen. Die Kupferionen befinden sich in dem Elektrolyten, der aus einer wässrigen Lösung von Kupfer(II)-Sulfat mit der chemischen Formel CuSO4 besteht. CuSO4 wiederum besteht aus einem Kupferatom, einem Schwefelatom und vier Sauerstoffatomen, womit die Masse einer einzelnen CuSO4-Komponente zu Die in einer Batterie gespeicherte Energiemenge wird meistens in Amperestunden (Ah) oder Milliamperestunden (mAh) angegeben. Eine Amperestunde ist die Ladungsmenge, die von einem konstanten Strom von einem Ampere in einer Stunde transportiert wird. Damit entspricht eine Amperestunde einer Ladung von 3600 Coulomb (Amperesekunden). Um die entsprechende Energiemenge zu errechnen, muss dieser Wert mit der Ausgangsspannung der Batterie multipliziert werden. InnenwiderstandWie weiter oben bereits erwähnt, hängt die Reaktionsrate von Hin-und Rückreaktion einer Halbzelle von den Konzentrationen des Edukts beziehungsweise der Produkte ab. Durch Änderung der Konzentration der Produkte ändert sich auch die Reaktionsrate der Rückreaktion. Die in der Tabelle der Normalpotentiale aufgelisteten Werte gelten für den Gleichgewichtsfall. Sobald die Pole der oben beschriebenen Zink-Kupfer-Batterie an einen Verbraucher angeschlossen werden, fließt ein elektrischer Strom und die Anzahl der Elektronen an der Zinkelektrode wird um eine entsprechende Rate erniedrigt. Je kleiner der Widerstand des Verbrauchers, desto mehr Elektronen werden in einem entsprechenden Zeitintervall "abgesaugt". An der Kupferelektrode verlassen Cu2+-Ionen den Elektrolyten, indem diese die Elektronen der Zinkelektrode aufnehmen. Um den Stromfluss aufrecht zu erhalten, muss eine entsprechende Zahl an Cu2+-Ionen nahe der Kupferelektrode sein, um den Elektrolyten verlassen zu können. Nimmt die Konzentration der Cu2+-Ionen rund um die Elektrode ab, so steigt die Rate der Hinreaktion an, womit pro Zeiteinheit weniger Cu2+-Ionen zu Kupfer reduziert werden:Als Konsequenz der steigenden Reaktionsrate der Hinreaktion sinkt die Ausgangsspannung der Batterie! Die Bewegungsgeschwindigkeit der Cu2+-Ionen beeinflusst die Reaktionsrate an der Kupferelektrode: 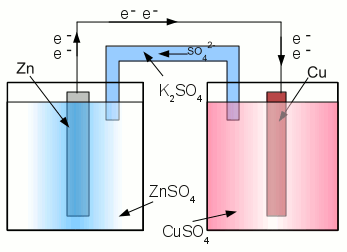 Zink-Kupfer Batterie:
Zink-Kupfer Batterie:Wird ein elektrischer Verbraucher an den Polen einer Batterie angeschlossen, führen die chemischen Reaktionen innerhalb der beiden Halbzellen zu einer ungleichmäßigen Verteilung der Ionen um die Elektroden herum. Die Konzentration der Zn2+-Ionen rund um die Anode steigt, die der Cu2+Ionen um die Kathode sinkt. Sobald ein elektrischer Verbraucher an eine Batterie angeschlossen wird, ist die Ausgangsspannung kleiner als bei unbelasteter Batterie. Die Differenz ist der Spannungsabfall am Innenwiderstand der Batterie. <<< Korrosionsschutz Batterietypen >>> Neuigkeiten Das Projekt Technik RoboSpatium Unterstützung Stichwortverzeichnis Archiv Download Reaktionen Spiele Verweise Gadgets Kontakt Impressum |
|
|