|
|
|
|
Neuigkeiten Das Projekt Technik RoboSpatium Unterstützung Stichwortverzeichnis Download Reaktionen Spiele Gadgets Kontakt <<< Batterietypen Viertakter >>> AkkumulatorenLadevorgangIn den vorangegangenen Kapiteln haben wir über die chemischen Prozesse in galvanischen Zellen gesprochen. Sobald man einen Verbraucher an die Pole einer Batterie anschließt, wird chemische Energie in elektrische Energie umgewandelt. Was ist nun mit dem umgekehrten Prozess - der Umwandlung von elektrischer in chemische Energie? Nun, man kann nicht einfach eine normale Batterie an eine Spannungsquelle anschließen, um den umgekehrten Prozess auszulösen, aber es gibt spezielle Batterien, die auf diese Art erneuert werden können!Wie wir in vorangegangenen Kapitel gelesen haben, ist Zink ein oft verwendetes Anodenmaterial in Batterien. Beim Entladen werden die Zinkatome zu Zn2+ Kationen oxidiert und gehen in Lösung. Die Zinkanode fungiert dabei als negativer Pol der Batterie. Um den umgekehrten Prozess auszulösen, muss die Anode an den Minuspol einer Gleichspannungsquelle angeschlossen werden und die Kathode an den Pluspol. Die Gleichspannungsquelle muss eine höhere Spannung bereitstellen als die Batterie. Andernfalls würden weiterhin Elektronen von der Anode der Batterie in den Minuspol der Spannungsquelle fließen, was zu einer weiteren Entladung der Batterie führen würde. Der dabei beabsichtigte Umkehrprozess ist: Zn2+(aq) + 2e- → Zn(s) Wenn wir einen Blick auf die elektrochemische Spannungsreihe werfen, sehen wir was tatsächlich passiert:2H3O+(aq) + 2e- → H2(g) + 2H2O Bedenkt, dass sich die Zn2+ Kationen in einer wässrigen Lösung befinden. Wasser zerfällt darin in Hydronium- und Hydroxidionen. Während unseres Ladeversuchs wirkt die Zinkelektrode wie die Kathode bei einem Elektrolyseprozess. Geraten Hydroniumionen in Kontakt mit der Zinkelektrode, werden diese zu elementaren, gasförmigen Wasserstoffmolekülen reduziert und das vorrangig vor den Zinkionen, da das Normalpotential der Hydroniumionen (0V) höher ist als das der Zn2+ Ionen (-0,76V). Das Resultat is die Produktion von Wasserstoffgas anstelle von elementarem Zink. Versucht also niemals, normale Batterien wieder aufzuladen - sie könnten dabei explodieren!Wie bereits erwähnt, gibt es jedoch spezielle Batterien, deren elektrochemische Vorgänge umkehrbar sind. Eine derartige Zelle nennt man Sekundärzelle, im Gegensatz zur nicht wiederaufladbaren Primärzelle einer Batterie. Weitere Bezeichnungen hierfür sind wiederaufladbare Batterie, Akkumulator oder kurz Akku. Um Energie in einer derartigen Akkuzelle zu speichern, muss diese mit einer Gleichspannungsquelle verbunden werden. Der Minuspol der Spannungsquelle wird mit dem Minuspol der Batterie und ebenso werden die beiden Pluspole miteinander verbunden. Die Spannung der Gleichspannungsquelle muss dabei höher als die der angeschlossenen Batterie sein. Die nun ablaufenden Prozesse ähneln denen im Kapitel Elektrolyse. Angetrieben von der elektrischen Energie der Gleichspannungsquelle, wird das Material an der Kathode reduziert und das an der Anode oxidiert. Das Kathodenmaterial besitzt dabei das niedrigere Normalpotential. Innerhalb der Zelle bewegen sich Anionen zwischen den Halbzellen, um den Ladungsausgleich herbeizuführen. 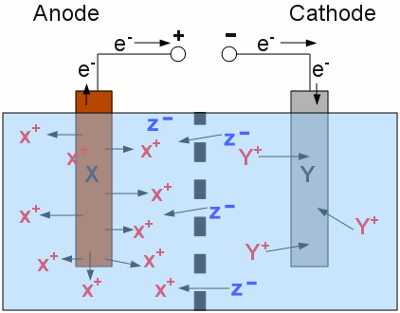
Ladevorgang eines Akkumulators: Die beiden Halbzellen der Akkuzelle sind durch einen Separator (Membran) voneinander getrennt und die Metallelektroden sind an eine Gleichspannungsquelle angeschlossen. An der Anode wird Metall X oxidiert (elementare Metallatome X gehen als X+ Kationen in Lösung) und an der Kathode wird Metall Y reduziert (Y+ Kationen werden als elementare Metallatome Y abgeschieden). Negativ geladene Anionen diffundieren von der rechten in die linke Halbzelle, um die Ladungsbilanz auszugleichen. Im Verlauf des Ladevorganges nimmt die Anzahl der X+ Kationen in der linken Halbzelle zu und die der Y+ Kationen auf der rechten Seite ab. Metall X besitzt dabei ein höheres Normalpotential als Metall Y, weswegen elektrische Energie aufgewendet werden muss, um chemische Energie im Verlauf dieses Prozesses zu speichern. Der Ladevorgang muss beendet werden, sobald sich keine Kationen mehr an der Kathode der rechten Halbzelle befinden beziehungsweise das gesamte Anodenmaterial in Kationen verwandelt worden ist. Bleibt die Zelle dennoch an die Gleichspannungsquelle angeschlossen, so treten unerwünschte Effekte auf. Befindet sich Wasser in der Zelle (um die Kationen zu lösen), werden die H2O Moleküle in gasförmige H2 und O2 Moleküle gespalten. Diese Mischung aus Wasserstoff und Sauerstoff ist hochexplosiv! Die Ladevorgänge unterschiedlicher Akkumulatoren wird in den folgenden Kapiteln über die jeweiligen Akkutypen besprochen. EntladevorgangBeim Entladevorgang werden die elektrochemischen Vorgänge innerhalb der Zelle umgekehrt.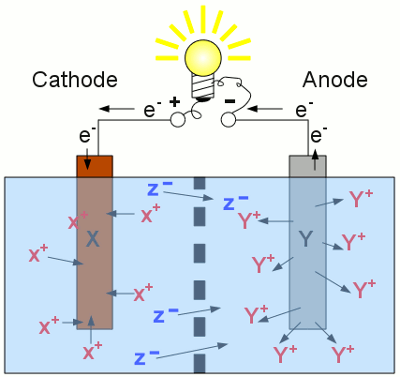
Entladevorgang einer Sekundärzelle: Sobald ein elektrischer Verbraucher an die Pole der Sekundärzelle angeschlossen werden, laufen die umgekehrten Prozesse in den Halbzellen ab. Nun fungiert die linke Halbzelle als Kathode. Das Material mit dem höheren Normalpotential wird reduziert (die X+ Kationen werden als elementare X Atome abgeschieden) und das mit dem niedrigeren Normalpotential wird oxidiert (elementare Y Atome gehen als Y+ Kationen in Lösung). Verglichen mit dem Ladevorgang sind die Funktionen von Anode und Kathode vertauscht und die Elektronen sowie die negativ geladenen Anionen fließen in die entgegengesetzte Richtung. Die Konzentration der Y+ Kationen in der rechten Halbzelle nimmt zu, die der X+ Kationen in der linken Halbzelle ab. Der Entladevorgang stoppt, sobald sich keine weiteren X+ Kationen in der linken Halbzelle befinden oder das gesamte Elektrodenmaterial Y in Lösung gegangen ist. Für die Lebensdauer der Sekundärzelle ist es sehr von Vorteil, den Entladevorgang zu beenden bevor das gesamte Elektrodenmaterial aufgelöst ist! LadezustandWie bereits im Kapitel zu den Batterien erwähnt, gibt die Kapazität die Menge an elektrischer Energie an, die in einer elektrochemischen Zelle gespeichert ist. Der Ladezustand - im Englischen State Of Charge (SOC) - gibt den Prozentsatz an bereits/noch gespeicherter Energie während des Lade-/Entladevorganges an. Bezogen wird der Wert auf die maximal mögliche Kapazität der Zelle (0-100%). Der Umkehrwert (100%-SOC) gibt den Entladezustand an - im Englischen Depth Of Discharge (DOD).EntladekurveBetrachten wir die Ausgangsspannung eines Akkus, an den ein konstanter elektrischer Verbraucher angeschlossen ist: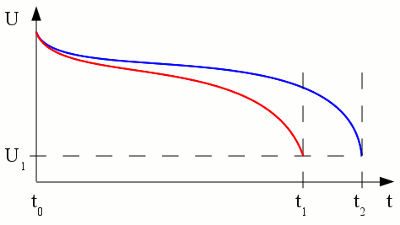
Spannungsverlauf für den Entladevorgang eines Akkus mit angeschlossenem, konstanten Verbraucher. Die Rote Kurve zeigt den Verlauf bei einem niederohmigen Verbraucher an (höherer Entladestrom). Wie wir sehen, ist die Ausgangsspannung im Verlauf der Entladung nicht konstant. Der Grund hierfür liegt in dem zunehmenden Innenwiderstand der Zelle (Details hierzu gibt's im Kapitel zu Batterien), hervorgerufen durch die abnehmende Konzentration der Kationen am der Kathode. Der Innenwiderstand der Zelle verursacht einen höheren Spannungsabfall, wenn ein stärkerer Verbraucher an die Pole des Akkumulators angeschlossen wird. Abhängig vom jeweiligen Batterietyp gibt es eine Ausgangsspannung, die im Verlauf der Entladung nicht unterschritten werden darf. Diese Spannung bezeichnet man als Entladeschlussspannung und wird hier im Zeitpunkt t1 beziehungsweise t2 erreicht. Zu diesen Zeitpunkten wird der Entladevorgang abgebrochen. Ein Entladen bis unterhalb der Entladeschlussspannung führt zu irreparablen Schäden in der Zelle! Kapazität und EntladestromWie im Kapitel über Batterien erklärt, ist die Kapazität einer Zelle ein fester Wert, der von den Stoffmengen in der Zelle abhängt. Der durch den Innenwiderstand hervorgerufene Spannungsabfall hängt von der fließenden Stromstärke ab. Wird der Akku nun mit einem relativ hohen Strom entladen, ist die entnehmbare Kapazität kleiner als erwartet, da die Entladeschlussspannung früHer erreicht wird. Die vom Hersteller angegebene Kapazität ist üblicherweise das Produkt aus 20Stunden mal dem Maximalstrom, den ein neuer Akku über eine Zeitdauer von 20 Stunden bei 20C° bereitstellen kann. Beträgt die aufgedruckte Kapazität 5Ah, so bedeutet das nicht, dass die Batterie einen Strom von 5A über eine Zeitdauer von einer Stunde bereitstellen kann. Es bedeutet, dass dieser Akku über eine Zeitdauer von 20Stunden einen Strom von 0,25A abgeben kannt - Zeit (in Stunden) über die der Akku den Strom liefern kann, QP - Kapazität bei 1A Entladestrom, I - Entladestrom, k - Konstante (circa 1.3) Somit verringert sich die Kapazität eines Blei-Säure Akkus mit 20Ah auf 10,02Ah beim Entladen mit 10A und auf gerade einmal 8,14Ah bei Entladung mit 20A! Ein weiterer Parameter, der die Kapazität beeinflusst ist die Umgebungstemperatur. Niedrige Temperaturen führen zu einer geringeren Diffusionsrate der Ionen und somit zum Ansteigen des Innenwiderstands, was schließlich zu einem weiteren Absinken der Kapazität führt. SelbstentladungSowohl Primär- als auch Sekundärzellen verlieren an Kapazität auch wenn kein Verbraucher angeschlossen ist. Diese Selbstentladung wird durch chemische Prozesse innerhalb der Zellen hervorgerufen. Primärzellen können in einem Jahr zwischen 8 und 20% ihrer ursprünglichen Kapazität verlieren.LebensdauerBei jedem Lade-/Entladezyklus eines Akkumulators treten Alterungsprozesse auf. Auch wenn der Akku nicht benutzt wird, wandern ständig Ionen von einer in die andere Halbzelle, da das Separatormaterial zwischen diesen niemals so selektiv arbeitet wie in der Theorie gefordert. Weiterhin wird das Elektrodenmaterial mit jedem Zyklus geschwächt und Teile davon können sich komplett ablösen. Ein weitere Seiteneffekt ist die Bildung von Kristallen in dem Elektrolyten oder auf der Elektrodenoberfläche. Der Separator kann durch Kristallbildung durchlöchert werden, was Kurzschlüsse hervorruft. All diese Effekte führen zu einer allmählichen Verringerung der Kapazität einer Zelle.KapazitätsausgleichNormalerweise besteht ein Akkumulator aus einer Reihenschaltung mehrerer elektrochemischer Zellen. Die Ausgangsspannung ergibt sich dann aus der Summe der Ausgangsspannungen der einzelnen Zellen.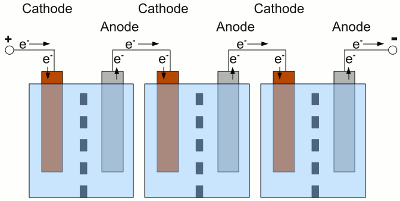
Reihenschaltung dreier elektrochemischer Zellen. Die dabei verwendeten Zellen sollten alle vom gleichen Typ sein, die gleiche Kapazität und einen identischen Ladezustand besitzen. Was passiert nun, wenn eine der Zellen komplett entladen ist, während die anderen Zellen noch über einen hohen Ladezustand verfügen? Die Zellen und der Verbraucher sind in Reihe geschaltet, also fließt durch alle Zellen der gleiche Strom: 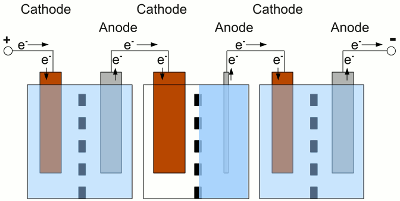
Die mittlere Zelle ist komplett entladen, die Nachbarzellen liefern jedoch weiterhin elektrische Energie. Aufgrund der Tatsache, dass die Nachbarzellen nach wie vor elektrische Energie bereitstellen, werden weitere Elektronen in die Kathode der entladenen Zelle gepumpt, auch wenn dort keine weiteren Metall-Kationen zu elementaren Metallatomen reduziert werden können. Wird Wasser als Lösemittel verwendet, erzeugen die nun ablaufenden Elektrolyseprozesse elementaren, gasförmigen Wasserstoff. An der Anode der entladenen Zelle werden weitere Elektronen abgesaugt und mehr Elektrodenmaterial als üblich geht als Ionen in Lösung. Verursacht dadurch kann die Elektrode zerbrechen. Der Prozess wird als Tiefentladung oder Umkehrladung bezeichnet, da die ablaufenden Vorgänge auch auftreten, wenn der Akku mit falscher Polung an ein Ladegerät angeschlossen wird. Auch wenn die mittlere Zelle nicht komplett entladen ist, aber der momentane Entladestrom hoch genug ist, kann an dem nun hohen Innenwiderstand der mittleren Zelle eine höhere Spannung abfallen, als diese generiert. Die Polarität der mittleren Zelle ist bei fließendem Strom umgekehrt. Je nach verwendetem Akkutyp können hierbei viele unerwünschte Nebenreaktionen auftreten, welche die Lebensdauer des Akkus herabsetzen. Um derartige Tiefentladungen einzelner Zellen zu vermeiden, müssen die Zellen beim Laden ausbalanciert (englisch "to balance") werden, um zu garantieren, dass alle Zellen des Akkus den gleichen Ladezustand besitzen. Die Überwachung der Ausgangsspannung einzelner Zellen während des Entladevorgangs ermöglicht es, eine schwache Zelle zu erkennen, bevor diese zerstört wird. Der Ladezustand kann über die Ausgangsspannung einer einzelnen Zelle oder des gesamten Akkumulators erkannt werden, sofern der fließende Strom bekannt ist. Der Entladevorgang muss beendet werden, sobald die Entladeschlussspannung einer Zelle oder des gesamten Akkus erreicht ist. Die Elektronik oder Software, die zur Überwachung der Ausgangsspannungen verwendet wird, bezeichnet man als Batteriemanagement. Aufgrund der komplexeren Hardware (Verkabelung) werden einzelne Zellen nur selten überwacht. Normalerweise wird die Ausgangsspannung des Akkumulators, also der Reihenschaltung mehrerer Zellen mit Hilfe der Elektronikschaltkreise überwacht. Der Nachteil dieser Methode liegt darin, dass eine einzelne defekte Zelle innerhalb eines Akkupacks nur schwer lokalisiert werden kann. WirkungsgradBeim Lade-/Entladevorgang treten stets Energieverluste auf, die durch den Innenwiderstand des Akkus hervorgerufen werden. Daher müssen wir neben den Verlusten im Ladegerät, der Steuerelektronik des Projektfahrzeugs und dem Wirkungsgrad des Elektromotors, ebenfalls die Verluste beim Laden und Entladen des Akkus beachten. Je nach Höhe des fließenden Stromes sind diese Verluste recht hoch!Daten zum Wirkungsgrad der einzelnen Akkutypen werden in den folgenden Kapiteln präsentiert. <<< Batterietypen Viertakter >>> Neuigkeiten Das Projekt Technik RoboSpatium Unterstützung Stichwortverzeichnis Archiv Download Reaktionen Spiele Verweise Gadgets Kontakt Impressum |
|
|