|
|
|
|
Neuigkeiten Das Projekt Technik RoboSpatium Unterstützung Stichwortverzeichnis Download Reaktionen Spiele Gadgets Kontakt <<< PSE Tabelle Redoxreaktion >>> ReaktionsgleichungenOktettregelWie bereits in einigen vorherigen Kapiteln erwähnt, ist die Elektronenkonfiguration der Edelgase sehr stabil. Außer Helium besitzen alle anderen Edelgase acht Valenzelektronen (das äußerste s-Orbital ist mit zwei und das äußerste p-Orbital mit sechs Elektronen gefüllt). Atome mit einer andere Anzahl an Valenzelektronen tendieren dazu, eine ähnliche Konfiguration zu erlangen, indem sie sich derartig mit anderen Atomen verbinden, dass sich ebenfalls acht Elektronen in ihrer äußersten Schale befinden. Das Bestreben eine Elektronenkonfiguration mit acht Valenzelektronen zu erreichen gilt speziell für die Hauptgruppenelemente (Gruppe 1, 2 und 13-17) und wird Oktettregel oder auch Edelgasregel genannt. Eine bekannte Ausnahme dieser Regel ist Wasserstoff, da die Edelgaskonfiguration der ersten Periode durch nur zwei Valenzelektronen ausgezeichnet ist, entsprechend der Elektronenhülle des Edelgases Helium. Die Tendenz, diese Konfiguration zu erreichen, wird als Duettregel bezeichnet. Lithium und Beryllium sind zwei weitere Elemente, die dieser Regel folgen.Chemische Reaktionen zwischen Atomen finden statt, um eine komplette 8er beziehungsweise 2er Konfiguration in der Außenschale zu erreichen. Die Haupttypen chemischer Bindungen sind kovalente und ionische Bindungen, wobei Elektronen abgegeben, aufgenommen oder gemeinsam verwendet werden. Lewis-FormelMoleküle mit ihren Atombindungen werden als Diagramme gezeichnet. 1916 hat der US-amerikanische Chemiker Gilbert Newton Lewis eine oft verwendete Symbolschreibweise veröffentlicht, welche die Valenzelektronen der Atome und ihre chemischen Bindungen in Molekülen zeigt. Er verwendete die chemischen Symbole für die Atome in der Struktur der Moleküle. Elektronen, die in Form einer chemischen Bindung den Elektronenhüllen beider Atome zugeordnet werden, sind dabei durch eine Linie zwischen den betreffenden Atomen dargestellt. Elektronen die nicht an einer chemischen Bindung beteiligt sind, werden als Punktpaare bei dem betreffenden Atom gezeichnet: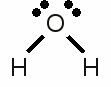 Lewis-Formel eines Wassermoleküls:
Lewis-Formel eines Wassermoleküls:Wasserstoff besitzt ein Valenzelektron, Sauerstoff besitzt sechs Valenzelektronen. Zwei der Valenzelektronen des Sauerstoffs bilden jeweils eine kovalente Bindung mit einem Wasserstoffatom, was durch Linien zwischen den betreffenden Atomen angezeigt wird. Die Beiden Elektronenpaare, die nicht an einer Bindung beteiligt sind, werden als Punktpaare neben dem Symbol für Sauerstoff gezeichnet. In dem gezeichneten Wassermolekül besitzt das Sauerstoffatom acht Valenzelektronen: Zwei einzelne Elektronenpaare und zwei Elektronenpaare, die gemeinsam mit dem Wasserstoffatom verwendet werden. Jedes Wasserstoffatom besitzt zwei Elektronen in seiner Hülle in Form einer kovalenten Bindung mit dem Sauerstoffatom. Die Bedingungen der Oktett- beziehungsweise Duettregel sind erfüllt. Die Doppelbindung zwischen zwei Sauerstoffatomen ist durch zwei parallele Linien zwischen ihren chemischen Symbolen und die nicht an einer chemischen Bindung beteiligten Elektronenpaare sind durch Punktpaare gekennzeichnet. Jedes Sauerstoffatom besitzt acht Valenzelektronen (zwei einzelne Paare und zwei gemeinsam verwendete Paare in Form der Doppelbindung). Die hier verwendete Schreibweise bezeichnet man als Lewis-Formel, Lewis-Struktur oder Elektronenformel. IonAußer der gemeinsamen Verwendung von Elektronen in Form einer kovalenten Bindung, können Atome auch durch die Abgabe von Elektronen ihre Außenschale "leeren" oder durch Aufnahme von Elektronen "füllen". Ein Beispiel für eine derartige ionische Bindung ist Natriumchlorid. Das Natriumatom gibt dabei im Verlauf der chemischen Reaktion sein einzelnes Valenzelektron dauerhaft an das Chloratom ab, was zur Bildung eines positiv geladenen Natriumions und eines negativ geladenen Chlorions führt. Positiv geladene Atome nennt man Kationen, negativ geladene Ionen Anionen.Ein einzelnes Chloratom besitzt sieben Valenzelektronen. Durch Aufnahme eines weiteren Elektrons von dem Natriumatom bildet sich ein einfach negativ geladenes chlorid-Anion. Das Natriumatom hat sein einziges Valenzelektron abgegeben und bildet somit ein einfach positiv geladenes Natrium-Kation. Ionen können auch aus einer Kombination kovalenter und ionischer Bindungen bestehen. Ein Beispiel hierfür ist das Carbonat-Ion: 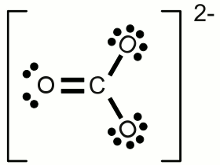 Zweifach negativ geladenes Carbonat-Ion:
Zweifach negativ geladenes Carbonat-Ion:Alle Atome die in dieser Molekül-Ion-Kombination vorhanden sind, besitzen acht Valenzelektronen. ReaktionsgleichungEine chemische Reaktion wird durch eine Reaktionsgleichung dargestellt. Die Ausgangssubstanzen oder Reaktanden werden auf der linken Seite geschrieben, getrennt durch einen oder zwei Pfeile von dem oder den Produkt(en) auf der rechten Seite. Die Pfeile zeigen die Richtung der Reaktion an. Wird Wasserstoff in einer sauerstoffhaltigen Atmosphäre verbrannt, so entsteht dabei Wasser nach der folgenden Reaktionsgleichung:Der Pfeil zeigt dabei von links (2H + O) nach rechts (H2O). Wir werden später noch sehen, dass Wasser auch nach der folgenden Gleichung in Wasserstoff und Sauerstoff aufgespalten werden kann: Erneut werden die Reaktanden auf der linken Seite (H2O) und die Produkte (2H + O) auf der rechten Seite geschrieben. Später werden wir noch sehen, dass die Reaktionsbedingungen manchmal auch die Reaktion in beide Richtungen erlaubt, was durch Doppelpfeile gekennzeichnet wird: 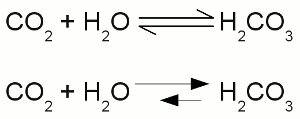 Chemische Reaktion in zwei Richtungen:
Chemische Reaktion in zwei Richtungen:Die obere Schreibweise wird verwendet, um das chemische Gleichgewicht anzuzeigen, was bedeutet, dass sich die Konzentration der Reaktanden und der Produkte im Verlauf der Zeit nicht ändert. Die untere Zeichnung zeigt, dass das Gleichgewicht (noch) nicht erreicht ist. Die Reaktionsrate der Rückreaktion (kleiner Pfeil nach links) ist kleiner als die Reaktionsrate der Hinreaktion (großer Pfeil nach rechts). Reaktanden und Produkte werden durch Pluszeichen voneinander getrennt und die an der Reaktion beteiligten Elemente beziehungsweise Substanzen werden durch ihre Verhältnisformel oder ihre Chemische Formel angegeben. Die Verhältnisformel einer chemischen Substanz ist das kleinstmögliche ganzzahlige Zahlenverhältnis der einzelnen Atome in diesem Stoff. Diese Formel wird für Stoffe mit ionischer Bindung wie zum Beispiel MgCl2 (Magnesiumchlorid) verwendet. Tiefgestellte Zahlen geben das Verhältnis der Elemente in dem Stoff an. MgCl2 bedeutet, dass Magnesiumchlorid aus Magnesium und Chlor im Verhältnis 1:2 besteht. Dieses Stoffmengenverhältnis kann durch chemische Analysemethoden bestimmt werden. Die Molekülformel oder auch chemische Formel gibt die Anzahl an Atomen eines betreffenden Elementes in einem einzigen Molekül an. Wie bei der Verhältnisformel gibt auch hier eine tiefgestellte Zahl an, dass das Molekül aus mehr als einem Atom des betreffenden Elements besteht. Ein einfaches, bereits mehrfach erwähntes Beispiel ist die chemische Formel von Wasser (H2O). Etwas komplexer ist das Molekül mit der Formel C6H8O7 (Zitronensäure) aufgebaut. Der Koeffizient direkt vor einem chemischen Symbol oder einer chemischen Formel bezeichnet die Anzahl der beteiligten Atome beziehungsweise Moleküle. Diese Zahlwerte bezeichnet man als stöchiometrische Koeffizienten. Mit deren Hilfe wird das Mengenverhältnis der Reaktanden und Produkte angegeben, wobei die kleinstmöglichen ganzzahligen Werte verwendet werden. Unter Berücksichtigung der Tatsache, dass Wasserstoff- beziehungsweise Sauerstoffgas aus Wasserstoff- beziehungsweise Sauerstoffmolekülen anstelle einzelner Atome besteht, ergibt sich die Reaktionsgleichung zu: 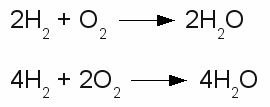 Stöchiometrische Koeffizienten:
Stöchiometrische Koeffizienten:Die Reaktion aus Wasserstoff und Sauerstoff ergibt Wasser. Das stöchiometrische Verhältnis von Wasserstoff, Sauerstoff und Wassermolekülen ist 2:1:2, was gleichbedeutend mit einem Verhältnis von 4:2:4 ist. Die obere Gleichung verwendet die kleinstmöglichen ganzzahligen Werte. Die Reaktionsgleichung wird gelesen als "Zwei H zwei plus O zwei ergibt H zwei O.". Die Anzahl der Atome eines Elements ändert sich im Verlauf einer chemischen Reaktion nicht, was als das Gesetz zur Erhaltung der Masse oder kurz Massenerhaltung bezeichnet wird. Damit muss sich die gleiche Anzahl an Atomen eines Elements auf beiden Seiten der Gleichung ergeben. Bei obigem Beispiel befinden sich 4 Wasserstoffatome ( = 2 * H * 2) und 2 Sauerstoffatome ( = 1 * O * 2) auf der linken Seite und ebenfalls 4 Wasserstoffatome ( = 2 * H *2O), sowie 2 Sauerstoffatome ( = 2 * H2O) auf der rechten Seite. Die untere Gleichung enthält 8 Wasserstoffatome ( = 4 * H * 2 ) und 4 Sauerstoffatome ( = 2 * O * 2 ) auf beiden Seiten. <<< PSE Tabelle Redoxreaktion >>> Neuigkeiten Das Projekt Technik RoboSpatium Unterstützung Stichwortverzeichnis Archiv Download Reaktionen Spiele Verweise Gadgets Kontakt Impressum |
|
|